Ca2+?EDTAХЉФъЄЮХЉФъЖЪРўЄђЩСЄЏЪ§ЫЁЄЫЄФЄЄЄЦЙЭЄЈЄоЄѓЄЭЄѓЁЃЄЄЄУЄСЄуЄѓЄЯЄИЄсЄЫЁЂEDTAЄЮЛРВђЮЅЄРЄБЄђЙЭЮИЄЗЄПОьЙчЄЮХЉФъЖЪРўЄђЩСЄЄоЄѓЄЭЄѓЁЃЄФЄЄЄЧЁЂCa2+ЄЮВУПхЪЌВђ(CaOH+ЄЮКјРИРЎ)ЄтЙЭЮИЄЫЦўЄьЄЦЄтЄІЄСЄгЄУЄШИЗЬЉЄЪЗзЛЛЄђЄЗЄЦХЉФъЖЪРўЄђЩСЄЄоЄѓЄЭЄѓЁЃЁЁЁЁЁЁ
EDTAЄЮЛРБіД№ШПБўЄРЄБЄђЙЭЮИЄЗЄПОьЙч
САВѓ(2024-05-05)НвЄйЄПЄшЄІЄЫЁЂCa2+ЄШEDTA(Y4-)ЄЮКјРИРЎШПБўЄЊЄшЄгКјРИРЎФъПєKfЄЯМЁЄЮФЬЄъЄфЁЃ
Ca2+ Ём Y4- ? CaY2-
Kf = [CaY]/([Ca][Y])
АьЪ§ЁЂY4-ЄЯБіД№ЄШЄЗЄЦЄЮРМСЄђЛ§ЄСЁЂЛРБіД№ШПБўЄЫЄшЄъY4-, HY3-, H2Y2-,
H3Y-, H4YЄЮВНГиМяЄЌЭЯБеЄЮpHЄЫБўЄИЄЦЄЂЄыГфЙчЄЧРИЄИЄоЄѓЄЭЄѓЁЃЄГЄЪЄЄЄЪЩїЄЪЁЂТаОнЄШЄЙЄыМчШПБў(КјРИРЎШПБў)АЪГАЄЮШПБўЄЯЩћШПБўЄШИЦЄаЄьЄЯЄъЄоЄЙЁЃ
Ca2+ЄШШПБўЄЗЄЦЄЊЄщЄиЄѓEDTAЄЮСДЧЛХйЄђ[YЁЧ], Y4-ЄЮТИКпЪЌЮЈЄђfy(=f0)ЄШЄЙЄыЄШЁЂМЁЄЮДиЗИЄЌРЎЮЉЄЗЄоЄУЄЛЁЃ
[YЁЧ] = [Y]Ём[HY]Ём[H2Y]Ём[H3Y]Ём[H4Y]
fy = [Y]/[YЁЧ]
ТИКпЪЌЮЈfyЄЯ[H]ЄЮЄпЄЮДиПєЄфЁЃЄЗЄПЄЌЄСЄІЁЂЄГЄГЄЧЄтЄЗpHЄЌАьФъЄфЄУЄПЄщЄаЁЂfyЄЯФъПєЄШЄЪЄыЄѓЄЧЄЙЄяЁЃЄГЄЮЄШЄЁЂ
Kf = [CaY]/([Ca][Y]) = [CaY]/([Ca][YЁЧ]fy)
ЄГЄГЄЧЁЂKffyЄђKfЁЧЄШЄЙЄыЄШЁЂ
KfЁЧ = [CaY]/([Ca][YЁЧ])
KfЁЧЄЯОђЗяРИРЎФъПєЄШИЦЄаЄьЄЯЄъЄоЄЙЁЃЁЁЁЁЁЁ
Cmo
mol/LЄЮCa2+ЄђДоЄрЭЯБеVmЄЫДЫОзБеЄђВУЄЈЄЦpHЄђАьФъЄЗЄЦТЮРбЄђV mLЄЫЄЗЄПЄЂЄШЁЂCyo mol/LЄЮEDTAЄЧХЉФъЄЗЄПЄШЄ(ХЉВМЮЬЁЇT
mL)ЄЮХЉФъЖЪРўЄђЕсЄсЄоЄѓЄЭЄѓЁЃЄГЄГЄЧЄЯEDTAЄЮЛРБіД№ШПБўЄРЄБЄђЩћШПБўЄШЄЗЄЦЙЭЮИЄЗЄоЄУЄЛЁЃ
ХЉФъЄЮГЦУЪГЌЄЫЄЊЄБЄыШяХЉФъЭЯБеУцЄЮCa2+ЄЮСДЧЛХйЄђCm mol/L,
EDTAЄЮСДЧЛХйЄђCy mol/LЄШЄЙЄыЄШЁЂХЉФъУцМЁЄЮДиЗИЄЌРЎЮЉЄЗЄоЄУЄЛЁЃ
Cm = CmoVm/(V+T) = [Ca]Ём[CaY]
Cy = CyoT/(V+T) = [YЁЧ]Ём[CaY]ЁЁЁЁЁЁ
АЪОхЄЮДиЗИМАЄЋЄщЁЂМЁЄЮЄшЄІЄЪХЉВМЮЬTЄШ[Ca]ЄЮДиЗИМАЄЌРЎЮЉЄЗЄоЄЙ(2024-05-05)ЁЃ
[Ca]2Ём(Cy?CmЁм1/KfЁЧ)[Ca]?Cm/KfЁЧ = 0
ЄГЄЮЦѓМЁЪ§ФјМАЄђВђЄЄЄЦ[Ca]ЄђЕсЄсЄоЄѓЄЭЄѓЁЃ
[Ca] = {(Cm?Cy?1/KfЁЧ)+Ђх((Cm?Cy?1/KfЁЧ)2Ём4Cm/KfЁЧ)}/2ЁЁЁЁЁФ?
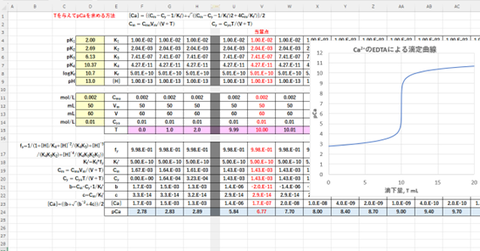
pCa=?log[Ca]ЄђЕсЄсЁЂT-pCaЄЮХЉФъЖЪРўЄђЩСЄЄоЄѓЄЭЄѓЁЃЁЁЁЁЁЁЁЁ
ЮуТъЃБЁЁCmo=0.002
mol/LЄЮCa2+ЅЄЅЊЅѓЄђДоЄрЭЯБеVm=50
mLЄЫpHДЫОзБе(KOH)ЄђВУЄЈЄЦV=60 mLЄЫЄЗЄПИхЁЂCyo =0.01 mol/LЄЮEDTAЄЧХЉФъЄЙЄыЄУЄСЄІЄШЄ(ХЉВМЮЬЁЇT
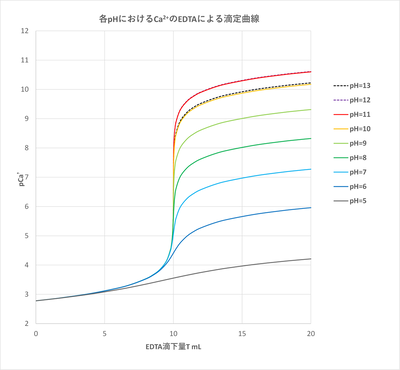
mL)ЄЮХЉФъЖЪРў(T-pCa)ЄђЕсЄсЄшЁЃpHЄЯ13.0ЄШЄЙЄыЄСЄІЄяЄБЄфЁЃCaOH+ЄЮРИРЎЄЯЙЭЮИЄЛЄѓЁЃЁЁЁЁЁЁ
ЭбЄЄЄПЪПЙеФъПєЄЯМЁЄЮФЬЄъ(ЅЄЅЊЅѓЖЏХйІЬЁс0.1ЄЮЄШЄЄЮУЭ)ЁЃ
ЁІEDTA(H4Y)ЄЮЛРВђЮЅФъПєЁЇ
K1 = [H][H3Y]/[H4Y]ЁЁ,ЁЁpK1 = 2.00
K2 = [H][H2Y]/[H3Y]ЁЁ,ЁЁpK2 = 2.69
K3 = [H][HY]/[H2Y]ЁЁ,ЁЁpK3 = 6.13
K4 = [H][Y]/[HY]ЁЁ,ЁЁpK4
= 10.37
ЁІCa-EDTAКјТЮЄЮКјРИРЎФъПєЁЇ
Kf = [CaY]/([Ca][Y])ЁЁ,ЁЁlogKf = 10.7
ЄГЄьЄщЄЮУЭЄЋЄщЁЂpH = 13.0ЄЫЄЊЄБЄыfyЄЊЄшЄгОђЗяРИРЎФъПєKfЁЧЄЯЁЂ
fy = [Y]/[YЁЧ] = 1/(1+[H]/K4+[H]2/(K4K3)+[H]3/(K4K3K2)+[H]4/(K4K3K2K1))
= 0.998
KfЁЧ = [CaY]/([Ca][YЁЧ])
= KffyЁЁ,ЁЁlogK fЁЧ = 10.65
ЄШЄЪЄыЄСЄІЄяЄБЄфЁЃ
?МАЄЊЄшЄгpCa=?log[Ca]ЄЋЄщЁЂЅЈЅЏЅЛЅыЄђЭбЄЄЄЦTЄЫТаЄЙЄыpCaЄђЕсЄсЄПЄСЄІЄяЄБЄфЁЃЗыВЬЄђПо-1ЄЫМЈЄЙЁЃЁЁЁЁЁЁ
EDTAЄЮЛРВђЮЅЄЊЄшЄгCaOH+ЄЮКјРИРЎЄђЙЭЮИЄЗЄПОьЙч
САЙрЄЧЄЯEDTAЄЮЛРБіД№ШПБўЄРЄБЄђЩћШПБўЄШЄЗЄПЄѓЄфЄЌЁЂЄГЄГЄЧЄЯEDTAЄЮЛРБіД№ШПБўЄЫВУЄЈЄЦCaOH+ЄЮКјРИРЎШПБў(ВУПхЪЌВђ)ЄтЙЭЮИЄЫЦўЄьЄЯЄъЄоЄЙЁЃЄЗЄПЄЌЄСЄІЁЂСАЙрЄЮДиЗИМАЄЮЄІЄСЁЂCmЄЫЄФЄЄЄЦЄЯЁЂ
Cm = CmoVm/(V+T) = [Ca]Ём[CaOH]Ём[CaY]
Ca-OHКјТЮЄЮРИРЎФъПєЄђІТoЄШЄЙЄыЄШЁЂ
ІТo = [CaOH]/([Ca][OH])
Cm = [Ca](1ЁмІТo[OH])Ём[CaY]
ЄЌРЎЮЉЄЗЄоЄУЄЛЁЃ
Y4-ЄШШПБўЄЗЄЦЄЊЄщЄиЄѓЅЋЅыЅЗЅІЅрЄЮСДЧЛХйЄђ[CaЁЧ]ЄШЄЗЁЂCa2+ЄЮТИКпЪЌЮЈЄђfmЄШЄЙЄыЄШЁЂ
[CaЁЧ] = [Ca]Ём[CaOH] = [Ca](1ЁмІТo[OH])
fm = [Ca]/[CaЁЧ] = 1ЁмІТo[OH]
ЄГЄЮЄШЄЁЂ
Kf = [CaY]/([Ca][Y]) = [CaY]/([CaЁЧ]fm[YЁЧ]fy)
Kffmfy = [CaY]/([CaЁЧ][YЁЧ])
ЄГЄГЄЧЁЂKffmfyЄђKfЁЧЁЧЄШЄЙЄыЄШЁЂ
KfЁЧЁЧ = [CaY]/([CaЁЧ][YЁЧ])
KfЁЧЁЧЄЯEDTAЄЮЩћШПБўЄЫВУЄЈЄЦCaOH+ЄЮРИРЎЄЫЄшЄыЩћШПБўЄтДоЄсЄПОђЗяРИРЎФъПєЄфЁЃfmЄтЄоЄП[H]ЄЮЄпЄЮДиПєЄфЁЃЁЁЁЁЁЁ
ШяХЉФъЭЯБеУцЄЮCa2+ЄЮСДЧЛХйЄђCm mol/L,
EDTAЄЮСДЧЛХйЄђCy mol/LЄШЄЙЄыЄШЁЂХЉФъУцМЁЄЮДиЗИЄЌРЎЮЉЄЗЄоЄУЄЛЁЃ
Cm = CmoVm/(V+T) = [CaЁЧ]Ём[CaY]
Cy = CyoT/(V+T) = [YЁЧ]Ём[CaY]ЁЁЁЁЁЁ
АЪОхЄЮДиЗИМАЄЋЄщЁЂХЉВМЮЬTЄШ[CaЁЧ]ЄЮДиЗИМАЄЌЕсЄоЄыЄѓЄф(*1)ЁЃ
[CaЁЧ]2Ём((Cy?Cm)Ём1/KfЁЧЁЧ)[CaЁЧ]?Cm/KfЁЧЁЧ = 0
[CaЁЧ] = {(Cm?Cy?1/KfЁЧЁЧ)+Ђх((Cm?Cy?1/KfЁЧЁЧ)2Ём4Cm/KfЁЧЁЧ)}/2ЁЁЁЁЁФ?
(*1) ?МАЄЯ?МАЄЮ[Ca], KfЁЧЄђЄНЄьЄОЄь[CaЁЧ], KfЁЧЁЧЄЫУжЄДЙЄЈЄьЄаЁЂМАЄЯЦБЄИЗСЄШЄЪЄыЄСЄІЄяЄБЄфЁЃЁЁЁЁЁЁ
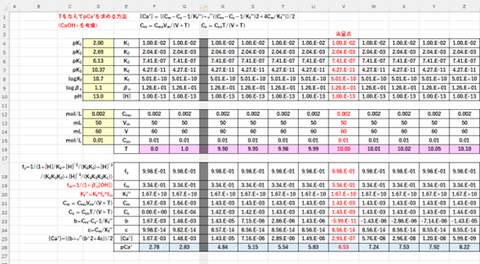
ЮуТъЃВЁЁЮуТъЃБЄШЦБЄИОђЗяЄЧЁЂCa2+ЄђEDTAЄЧХЉФъЄЙЄыЄУЄСЄІЄШЄ(ХЉВМЮЬЁЇT
mL)ЄЮХЉФъЖЪРў(T-pCaЁЧ)ЄђЕсЄсЄшЁЃЄЛЄфЄБЄЩЁЂCaOH+ЄЮРИРЎЄђЙЭЮИЄЙЄыЄСЄІЄяЄБЄфЁЃЁЁЁЁЁЁ
ЁІEDTA(H4Y)ЄЮЛРВђЮЅФъПєЁЇ
pK1 = 2.00
pK2 = 2.69
pK3 = 6.13
pK4 = 10.37
ЁІCa-EDTAКјТЮЄЮРИРЎФъПєЁЇ
logKf = 10.7
ЁІCa-OHКјТЮЄЮРИРЎФъПєЁЇ
ІТo = [CaOH]/([Ca][OH]),ЁЁЁЁlogІТo =
1.1
ЁІПхЄЮЅЄЅЊЅѓРбЁЇЁЁpKw
= 13.8
ДиЗИМАЄЯЁЂ
KfЁЧЁЧ = [CaY]/([CaЁЧ][YЁЧ]) = Kf(fmfy)
Cm
= CmoVm/(VЁмT) = ([Ca]Ём[CaOH])+[CaY] = [CaЁЧ]+[CaY]
Cy
= CyoT/(VЁмT) = [YЁЧ]Ём[CaY]
fm = [Ca]/[CaЁЧ] = 1/(1ЁмІТo[OH]) = 1/(1+ІТoKw/[H])
fy = [Y]/[YЁЧ]
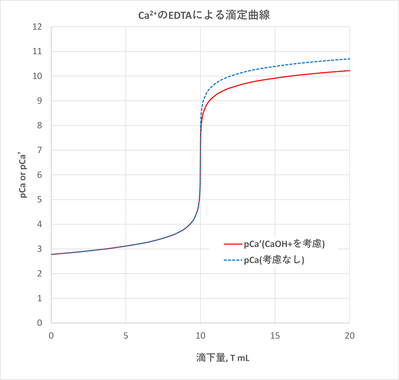
?МАЄЊЄшЄгpCaЁЧ=?log[CaЁЧ]ЄЋЄщЁЂЅЈЅЏЅЛЅыЄђЭбЄЄЄЦTЄЫТаЄЙЄыpCaЁЧЄђЕсЄсЄПЄСЄІЄяЄБЄфЁЃЗзЛЛЗыВЬЄђПо-ЃВЄЫМЈЄЗЁЂХЉФъЖЪРўЄђПо-ЃГЄЫМЈЄЙ(РжПЇЄЮМТРў)ЁЃПо-ЃГУцЄЫЄЯЮуТъЃБЄЮЗыВЬЄтМЈЄЙ(РФПЇЄЮХРРў)ЁЃЁЁЁЁЁЁ
CaOH+ЄђЙЭЮИЄЙЄыЄШЁЂЙЭЮИЄЛЄЪЄЄЫШцЄйЄЦЁЂХіЮЬХРИхЄЫEDTAЄШЬЄШПБўЄЮCaЮЬЄЌС§ВУЄЙЄы(pCaЁЧЄЌИКОЏЄЙЄы)ЄГЄШЄЌЪЌЄЋЄыЄѓЄфЁЃЁЁЁЁЁЁ
pHЄЫЄшЄыK''ЄЊЄшЄгХЉФъЖЪРўЄЮЪбПШ
Ca-EDTAКјТЮЄЮОђЗяРИРЎФъПєKfЁЧЁЧЄЮДиЗИМАЄЯМЁЄЮФЬЄъЄфЁЃ
KfЁЧЁЧ = [CaY]/([CaЁЧ][YЁЧ]) = Kffmfy
fy = [Y]/[YЁЧ] = 1/(1+[H]/K4+[H]2/(K4K3)+[H]3/(K4K3K2)+[H]4/(K4K3K2K1))
fm = [Ca]/[CaЁЧ] = 1/(1ЁмІТo[OH])
= 1/(1+ІТoKw/[H])
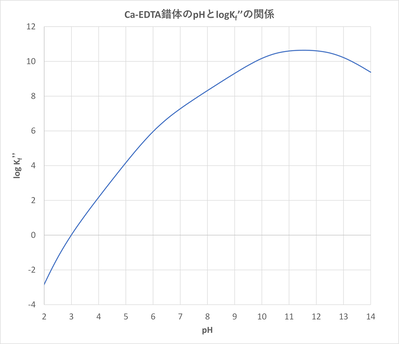
ЄГЄЮМАЄЧЁЂfmЄЊЄшЄгfyЄЯpHЄЮДиПєЄфЄЋЄщЁЂKfЁЧЁЧЄЯpHЄЫЄшЄУЄЦЪбПШЄЗЄоЄУЄЛЁЃ
ОђЗяРИРЎФъПє(Kf'')ЄШpHЄЮДиЗИЄђПо-ЃДЄЫМЈЄЗЄоЄУЄЛЁЃЄоЄПЁЂpHЄђЪбПШЄЕЄЛЄПЄШЄЄЮХЉФъЖЪРўЄЮЭЭЛвЄђПо-ЃЕЄЫМЈЄЗЄоЄЙ(*2)ЁЃ
(*2) По-ЃЕЄЯПо-ЃВЄЫМЈЄЗЄПЅЈЅЏЅЛЅыЅЗЁМЅШЄЋЄщЁЂWhat-IfЪЌРЯЄЮЅЧЁМЅПЅЦЁМЅжЅыЕЁЧНЄђЭбЄЄЄЦКюРЎЄЗЄПЄСЄІЄяЄБЄфЁЃЁЁЁЁЁЁ
ХЉФъРКХйЄђИўОхЄЕЄЛЄыЄПЄсЄЫЄЯKfЁЧЁЧЄЌТчЄЄЪЄыpHЄђСЊЄжЩЌЭзЄЌЄЊЄоЄЙЁЃEDTAЄЫЄшЄУЄЦCa2+ЄђХЉФъЄЙЄыЄУЄСЄІЄШЄЄЮКЧХЌpHЄЯ10?13ФјХйЄЧЄЂЄыЄГЄШЄЌЪЌЄЋЄыЄѓЄфЁЃЁЁЁЁЁЁ
ЅГЅсЅѓЅШ